ブランク(空白期間)は転職で不利?期間別の影響や病気が原因の伝え方

会社を辞めてから転職するまでの期間はブランク(空白期間)となります。
そこで当記事ではブランクのある状態で転職をする人に向けて、空白期間別の影響や注意点、やむを得ない事情でブランクがある場合の説明方法などを紹介します。
ブランクありの転職を検討している方は、ぜひ当記事を参考にして下さい。
ブランク(空白期間)があると転職で不利になる?
結論から言うと、ブランク(空白期間)がある状態での転職は残念ながら不利になることが多いです。
ただ、ブランクが短期間であればそれほど転職に影響はありません。
基本的には空白期間が長引けば長引くほど、転職時の書類選考や面接で不利になると思いましょう。
空白期間別の転職への影響
では、具体的に空白期間の長さが転職にどれくらいの悪影響を及ぼすのか、ブランク期間別に見ていきましょう。
1ヶ月以内
転職までのブランクが1ヶ月以内の場合は、ほとんど影響がないと言えるでしょう。
これは転職活動をする方の大半は1ヶ月以上、転職活動をしているため、企業も1ヶ月程度のブランクであればあまり気にしないからです。
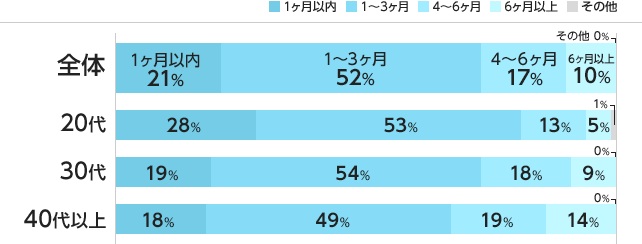
実際、エン転職の「転職活動」についてのアンケート調査によると、「実際の転職活動にかかった期間はどのぐらいでしたか?」という質問に対して、1ヶ月以内が21%、1~3ヶ月が52%と、求職者の7割以上が3ヶ月以内に転職を決めています。
参考:エン転職「転職活動」について
1~3ヶ月
ブランクが1~3ヶ月ある場合も、あまり気にしない企業が多いです。
ただ3ヶ月になるとブランクを気にし始める企業も出てきますので、可能であれば退職後1~2ヶ月以内に転職を決めるのが無難と言えます。
より言ってしまうと、在職中に転職を活動をして、転職先が決まってから退職をした方がよりスムーズです。
3~6ヶ月
退職後6ヶ月になると、企業の採用担当者や面接官の見る目が微妙に変わってくるため、転職に悪影響が出始めます。
3か月以内に転職活動を終える方が多いため、6ヶ月となると「どうして半年も転職が決まらなかったのだろう?」「何か転職できない理由があるのではないか?」という懸念が、企業側に生まれてくるからです。
「ブランクが6ヶ月間ありますが、その間は何をしていましたか?」といった質問を受けることも多くなるでしょう。
ただ、しっかりと6ヶ月ほどのブランクがある理由を伝えることができれば、まだまだ採用される可能性は十分にあります。
6ヶ月~1年
この辺りから本格的に転職への悪影響が出ます。
1年近くブランクがあると、相応の理由がなければ大半の企業は採用を敬遠します。
何らかの問題がある人材と判断されるため、ブラック企業でもない限り書類選考で落とされてしまう可能性が高いでしょう。
「留学」や「家族の介護」など1年近いブランクがある理由をしっかりと応募書類で説明できれば別ですが、何もしていないで1年のブランクがあると採用はかなり厳しいと思いましょう。
2年以上
空白期間が2年以上ある場合、家族の介護や病気といった正当な理由があった場合も転職はかなり不利になってしまうでしょう。
ブラック企業ですら書類選考で落とされてしまう可能性が高く、特に正社員としての転職はかなり厳しいです。
正社員でなく一度派遣やパートの雇用形態での就職を目指す、在宅ワークで稼ぐなど方向転換をするのがおすすめです。
ブランク(空白期間)で転職を不利にしない方法
ここからは実際にブランクがある方が、転職を成功させる方法を紹介していきます。
堂々と面接や試験に臨む
ブランク期間が長いほど書類選考で落ちまくるため、自信を喪失してしまいがちですが、臆せず堂々と面接や採用試験を受けるようにして下さい。
ネガティブになった状態で転職活動を成功させることは、不可能と言ってもいいでしょう。
空白期間を不利にしないためには、たとえブランクが長くても自分の可能性を信じて堂々と面接に挑むことが大切です。
仮に1年のブランクがあったとしても、自分なりに頑張っていることをしっかり面接官に伝えることが大切です。
ブランクによって自分が成長したことを伝える
長いブランク期間があっても転職を不利にしないためには、理由を説明するだけではなくブランク期間によって自分がどう成長したかを伝える必要があります。
試験勉強をしていた、副業をやってスキルを磨いたなど、ブランク期間中に自分が成長に向けて努力していたことをしっかり面接官に伝えましょう。
何もせずに遊んでいたのでなく、成長のためのブランク期間だと納得してもらえれば、キャリアに長めの空白期間があっても面接官は納得するでしょう。
病歴がある場合は細心の注意を払って伝える
病気を理由に前職を辞めてブランクがある人は、それを応募先に伝える際は細心の注意を払って下さい。
たとえ正当な病気療養であっても、伝え方によっては企業に落とされてしまう可能性が高いからです。
企業は病気の社員を雇うと仕事に支障をきたしたり、労災が発生することを恐れているので、どうしても採用には及び腰になってしまいます。
病気によるブランクがあって転職する場合の伝え方
完治している場合
会社を辞めた時点では病気をしていたけれど、ブランク期間中に完治している場合は無理に病歴を記載する必要はありません。
法律的にも2017年に個人情報保護法が改正となったことで、病歴や身体障害・精神障害などは「要配慮個人情報」(保護法2条3項)として明確に保護されています。
そのため、法的に病歴を記載する義務は応募者にはありませんし、記載せずとも問題ないと考えて良いでしょう。
たとえ病気をした事実があっても体調が万全で問題なく働ける状態であれば健康な人と何ら変わりませので、聞かれた場合にだけ答えれば十分でしょう。
病気の治療中で、まだ完治していない場合
ブランク期間に病気の治療をしていたものの、まだ完治していない場合は法律的に問われることがないとしても書類に記載しておき、面接時にも伝えた方が無難です。
仮に転職時に病気のことがバレなくても入社後に病気が重くなって早退が続いた場合、採用担当者が前職に問い合わせて病歴がバレることで、会社との関係性が最悪になるからです。
また、精神疾患などで通院や服薬をしている場合も、通院していることが入社後にバレてトラブルに発展するケースは少なくありません。
そのため、採用後のリスクを回避する意味でも、療養中の場合は病気のことを採用担当者に伝えた方が無難です。
病気を伝えずに面接を受ける人がいるのも事実
ただ、病気でブランクのある求職者の中には、「疾患を伝えたら100%採用されないから、背に腹は代えられない」と考え、病歴を伝えずに採用試験を強行突破する人がいるのも事実です。
ただ、病気のことを何年も職場に完璧に隠し続けるのは不可能ですし、働きながらだと完治が遅れることが多いので、採用後のトラブルのリスクを考えると可能であれば完治するまで療養した方が無難です。
また、精神疾患の場合は完治したかどうかが本人も自覚できないケースも多く、ブランクからの社会復帰には医師のアドバイスをしっかりと受けることが大切です。
病歴を応募先から訊ねられた場合
応募先によっては、ブランクがあると自分から病歴を伝えるまでもなく、向こうから「既往歴はありませんか?」と訊ねてくるケースもあります。
この場合は、「内容に虚偽があると採用を取り消す」といった同意書を取り交わすことも多く、隠して入社をしてもバレた時に確実に解雇になるので病歴を離すべきです。
病歴があっても問題なく働けることを伝えるためには、医師の診断書を提出することも有効な方法です。
企業が応募者に既往歴を聞く場合、プライバシーの侵害や個人情報保護法違反にあたるリスクもあるため、むやみやたらと追及されることはないでしょう。
ただ、同意書を書いた後は応募者にも責任が生まれるため、その点については注意が必要です。
転職のブランク(空白期間)があっても好印象な回答例
ここからは転職のブランクがある場合でも、面接官に好印象を与えることができる答え方の例を紹介していきます。
ブランク中に勉強をしていたと伝える
空白期間ではITエンジニアの経験を積んで、入社後の業務を少しでもスムーズに行うために、基礎情報技術者の資格取得に向けて勉強をしていました。
来月受験予定ですが、ブランクの期間にIT業界の専門用語や基本的なIT知識を事前にインプットすることができ、良かったと思っています。
ブランク中に思考転換をしていたと伝える
在職中は仕事に追われていたため、退職後は自分のキャリアの棚卸しから始め、キャリアチェンジも視野に入れて、自分にはどんな仕事が向いているのかを時間をかけて考えました。
その結果、自分には営業の仕事ではなく、マーケティングの仕事が向いているのだという判断に至りました。
その後はマーケティングに関する本を読みあさり、マーケティング・ビジネス実務検定の勉強をして、転職に備えておりました。
ブランク中に自分の市場価値を高めていたと伝える
在職中は多忙を極めていたため、自分のやりたいことがまったくできない状態でした。
そのため、空白期間では気持ちをリセットし、以前からずっと行きたかったロサンゼルスに3ヶ月近く滞在して、英語力を身に着けたり視野を広げていました。
そのためブランク期間が長くなりましたが、今後グローバルに営業活動を行っていきたいと考えていたので、非常にいい経験になったと思っています。
転職でブランクがある場合の注意点
空白期間でも税金や確定申告が発生する
転職に空白期間が生じた場合であっても、住民税といった税金や確定申告の手間が発生する点には注意が必要です。
特に住民税は今までは給与から天引になっていたと思うのですが、空白期間中は自分で納めなくてはいけません。
つまり、ブランクが長引けば長引くほど税金で貯金が減っていくことになるので、可能であれば早めに転職先を決めた方が良いでしょう。
健康保険や年金の手続きが必要
日本では「国民皆保険」制度により全員が健康保険に加入しつつ、年金も支払う義務があるので、空白期間であっても手続きをして支払う必要がある点に注意して下さい。
働いている間は保険料や年金は給与から引き落とされていましたが、役所の窓口にいって「国民健康保険」、「国民年金」に切り替えなくてはいけません。
給料がないのに毎月支払わなくてはいけないだけでなく、収入によっては国民健康保険と国民年金で支払う金額は重いので要注意です。
期間が長引くほど転職で不利になる
先程も軽く説明しましたが、基本的にブランクの期間が長ければ長いほど転職で不利になる点にも注意しましょう。
1ヶ月程度のブランクであれば突っ込んでくる企業はまずありませんが、やはり3ヶ月・6ヶ月辺りから怪訝に思う企業が増えてきます。
1年を超えてしまうと書類選考の突破すら難しくなってしまうので、病気や介護といった致し方ない事情がない場合は1日でも早く転職を成功させた方が良いでしょう。
空白期間(ブランク)がある状態で転職を成功する方法
ここからは空白期間があるという不利な状態で、転職を成功させるための方法を紹介していきます。
空白期間があるとハローワークやタウンワークの活用といった、普通の手段では転職が成功し辛いため参考にして下さい。
転職サイトを活用
ブランクがある場合、ハローワークでなく転職サイトを活用して求人を探すのがおすすめです。
これは、転職サイトでは最初から「ブランクOK」「ブランク歓迎」といった条件で求人を出している企業が検索できるからです。
ブランクのある人材を歓迎している求人なので、当たり前ですがブランクがあっても書類選考で落とされることがありません。
普通にハローワーク経由で応募すると、ブランクがあっても良いか不明なので、応募してはブランクを理由に書類選考で落とされることの繰り返しになりますが、転職サイトであればその心配がないのは大きなメリットでしょう。
転職エージェントを活用
ブランクがある場合は転職サイトだけでなく、転職エージェントの活用もおすすめです。
転職エージェントの魅力は登録すると専属のコンサルタントが付くことで、ブランクがある旨を伝えるとブランクのある人材も歓迎の求人だけを紹介してもらえます。
転職サイトのように求人を自分で探す手間がかからず、希望があれば「土日休み」「残業なし」「年収500万以上」といった条件を満たした求人も紹介してもらえます。
もちろん利用は完全無料となっているので、ブランクがある方は転職サイト1社と転職エージェント1社を併用して、応募していくと良いでしょう。
ハローワークやタウンワークはおすすめしない
ちらっと触れましたが、ブランクがある方はハローワークやタウンワークでの転職はおすすめしません。
これはまず「ブランクOK」の求人を絞って検索できないので、応募しても書類選考で落とされて効率が悪いためです。
また、ハローワークやタウンワークは掲載が無料かつ、違法行為をしても特に罰則がないせいでブラック企業の求人が大量出ているのも理由です。
転職サイトや転職エージェントは企業が掲載料や紹介料を支払う必要があり、違法行為やブラック企業は掲載取り消しになるので、資金に余裕があってホワイトな会社が中心となっています。
そのため、ブラングがある方はハローワークやタウンワークを利用する意味がないでしょう。
転職のブランク(空白期間)や注意点まとめ
今回は転職のブランク(空白期間)がどのくらい転職活動に影響を与えるのかや、不利にならないための対処法などを紹介しました。
転職のブランク期間が長いからといって能力が低いわけではありませんが、転職で不利になる場面があるのは事実です。
ブランクがある方はなるべく早めに転職活動を行いつつ、転職サイト・エージェントなどを活用することで、転職に成功する確率を上げられるでしょう。










